
PROGETTI DI RICERCA SCIENTIFICA SOSTENUTI DALL’ASSOCIAZIONE NEL 2020
Come ormai tutti sappiamo l’associazione IL CUORE GRANDE DI FLAVIO – ODV sostiene annualmente i progetti di ricerca scientifica sui “SARCOMI PEDIATRICI” realizzati nei laboratori dell’Ospedale Bambin Gesù.
Negli ultimi due abbiamo potuto donare 50 mila euro annui (con un obiettivo triennale di 150 mila) grazie al contributo di quanti, come noi, credono nei progressi della scienza e sperano di poter garantire una cura ed un futuro ai bambini malati di tumore.
Per dimostrare a tutti voi la nostra gratitudine vogliamo condividere l’aggiornamento sui progetti attualmente in corso:
- Studio pilota per valutare l’uso della biopsia liquida nella stadiazione clinica e preclinica dei rabdomiosarcomi
In collaborazione con l’EpSSG (The European paediatric Soft tissue sarcoma Study Group) e l’ITCC (Innovative Therapies for Children with Cancer) partecipiamo ad uno studio pilota che ha lo scopo di rilevare e quantificare il DNA tumorale circolante nel sangue perferico di pazienti affetti da Rabdomiosarcoma.
L’obiettivo finale del progetto è di permettere un miglioramento della valutazione della malattia in modo non invasivo, ovvero attraverso un semplice prelievo di sangue. Questo permetterebbe di seguire l’evoluzione tumorale anche durante il trattamento.
Avanzamento attività: attualmente abbiamo reclutato presso il nostro centro 9 pazienti affetti Rabdomiosarcoma ed abbiamo analizzato il DNA tumorale circolante, sia libero nel plasma che contenuto negli esosomi (vescicole secrete dalle cellule), al momento della diagnosi ed a differenti momenti del trattamento chemioterapico. Le analisi sono in corso ed i dati ottenuti verranno confrontati con il DNA del tumore primitivo o delle metastasi, quando possibile.
I passi successivi saranno quelli di identificare delle mutazioni presenti nel DNA circolante che potranno essere monitorate nel corso del trattamento. In caso ci siano farmaci target per queste mutazioni potranno essere usati per il trattamento di questi tumori.
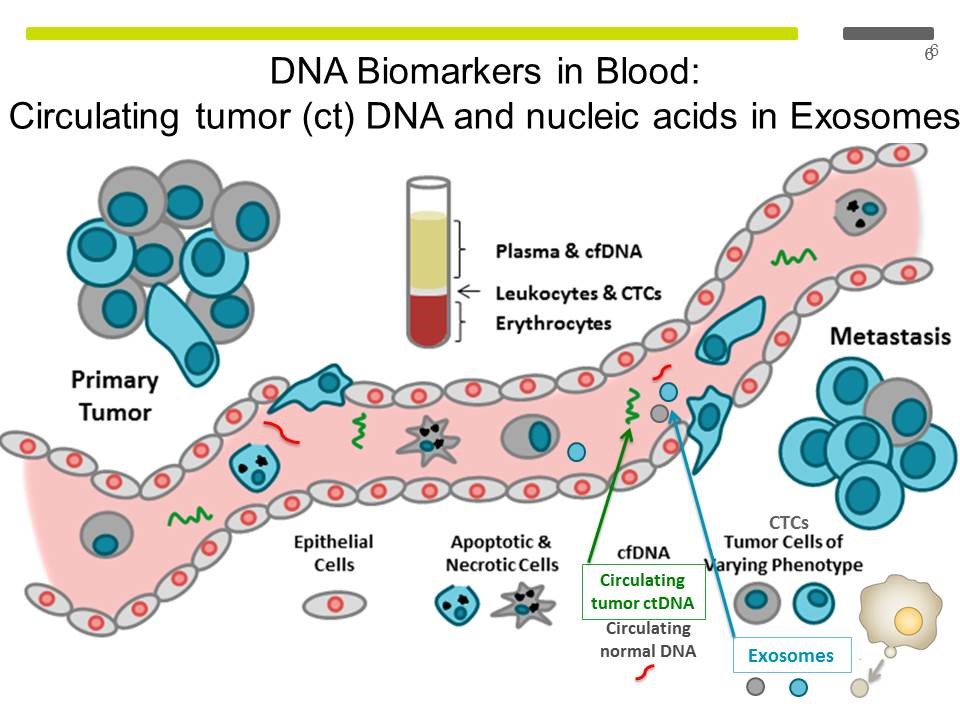
Figura rappresentante il concetto di biopsia liquida: gli esosomi (che contengono DNA) ed il DNA libero derivati dal tumore primitivo o dalle metastasi sono circolanti nel sangue periferico.
- Generazione di modelli animali di rabdomiosarcoma ed altri tumori pediatrici, Patient-Derived Xenograft (PDX)
I PDX sono dei modelli in vivo in cui frammenti di tessuto tumorale prelevati dal paziente al momento delle procedure chirurgiche vengono impiantati in topi immunocompromessi.
L’obiettivo finale del progetto è quello di generare un sistema che rispecchia la naturale crescita dei tumori pediatrici e che sia in grado di ricapitolare la patogenesi di questi tumori come il rabdomiosarcoma. Schema riassuntivo per la generazione dei PDX:
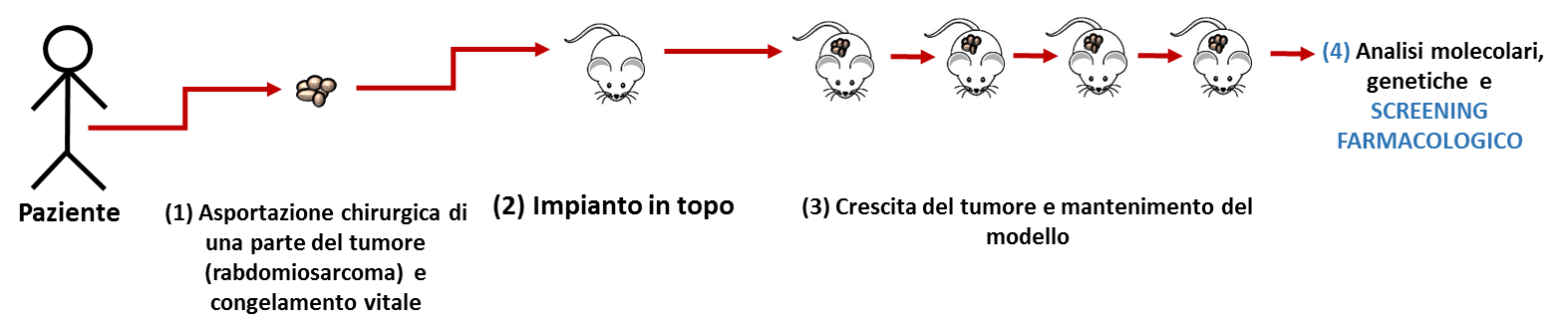
Risultati raggiunti: attualmente sono stati generati due PDX derivati da pazienti affetti da rabdomiosarcoma, un rabdomiosarcoma alveolare ed uno embrionale.
Passi successivi: effettuare degli screening farmacologici per testare l’efficacia di diversi farmaci in questi tumori in modo mirato, in particolare durante la recidiva.
- Espressione dell’Endoglin (CD105) come marcatore della vascolarizzazione tumorale nel Rabdomiosarcoma
La densità intratumorale dei microvasi rappresenta un parametro utilizzato per quantificare la vascolarizzazione tumorale. L’endoglin (CD105) è una proteina espressa in maniera predominante nell’endotelio vascolare in proliferazione e dà indicazioni sulla neovascolarizzazione.
L’obiettivo finale del nostro studio è stato quello di evidenziare una specifica espressione del CD105 nelle cellule endoteliali di tutti i campioni tumorali derivati da pazienti affetti da rabdomiosarcoma.
I risultati raggiunti hanno evidenziato che un incremento dell’espressione del CD105 correlava con una bassa sopravvivenza nei pazienti.
Passi successivi: abbiamo quindi deciso di incrementare la popolazione dello studio anche ad altri sarcomi pediatrici per valutare se questo marcatore possa essere utilizzato anche come marker di risposta alla terapia antiangiogenetica e target terapeutico. In particolare, abbiamo incluso nello studio, oltre a nuovi casi di Rabdomiosarcoma, Sarcomi di Ewing, Sarcomi Desmoplastici e Sarcomi indifferenziati che erano stati trattati con farmaci antiangiogenetici, come Pazopanib, associato a terapia convenzionale (Vincristina e Irinotecan).
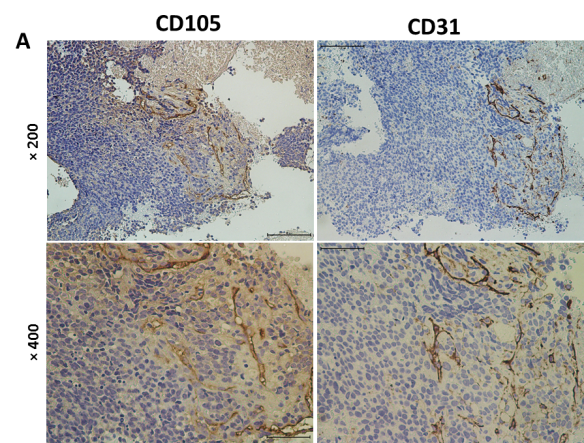
Immunostaining rappresentativo per CD105, CD31 in un paziente con Sarcoma di Ewing.
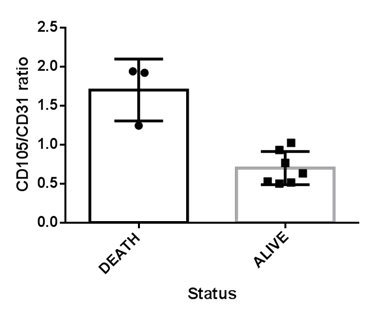
Correlazione tra il rapporto dell’espressione CD105/CD31 nei tessuti tumorali e lo stato dei pazienti.
- Profili di metilazione ed implicazione cliniche nei sarcomi pediatrici
Nel corso dell’ultimo anno, è stato messo a punto in OPBG un flusso di lavoro per la caratterizzazione molecolare dei sarcomi pediatrici (SP), analizzando per ogni singolo tumore il profilo di metilazione del DNA. In particolare, sono state svolte le seguenti attività:
1) Collezione sistematica di campioni di sangue
2) Analisi del profilo di metilazione del DNA tumorale mediante tecnologia Infinium su iScan (Illumina)
3) Creazione di database integrati molecolari/istopatologici dei sarcomi pediatrici con messa a punto di un sistema di classificazione molecolare basato su algoritmi di apprendimento automatico.
4) Comprensione del significato prognostico della nuova classificazione molecolare e delle implicazioni in ambito terapeutico.
5) Acquisizione di nuove conoscenze biologiche identificando le caratteristiche di espressione genica tumore- specifico derivanti dai meccanismi di metilazione aberranti.
I dati di metilazione del DNA sono complementari ad altre metodologie molecolari d’avanguardia, come il Next Generation Sequencing (NGS), che stanno sempre più prendendo piede nell’ambito della ricerca oncologica di base e traslazionale. Mentre il sequenziamento del DNA può rivelare potenziali bersagli terapeutici e marcatori diagnostici, il profilo di metilazione del DNA può inserire queste mutazioni nel giusto contesto di un tumore e di un’eventuale sottoclasse, e i due livelli di informazioni s’integrano efficacemente per la diagnosi, la prognosi e il trattamento ottimale del paziente pediatrico affetto da sarcoma.
La metodologia proposta vuole essere incorporata in un ambiente diagnostico di routine, risultando in un sostanziale miglioramento della precisione diagnostica anche in ambito di studi clinici mirati.
Per specifiche patologie, la ricaduta clinica è immediata. In particolare, i tumori primitivi a piccole cellule rotonde blu (SBRCT) dell’età pediatrica e dei giovani adulti rappresentano una sfida diagnostica e terapeutica. Il sarcoma di Ewing (ES) è il prototipo di un sarcoma indifferenziato con tale fenotipo, che, tuttavia, condivide con altre entità di sarcoma, assieme all’espressione di membrana di CD99 (Carter & Patel 2019). Un passo avanti nella diagnosi del sarcoma di Ewing è stata l’identificazione di traslocazioni bilanciate altamente specifiche che esitano in un gene chimerico fra membri della famiglia TET (principalmente EWSR1) e membri della famiglia ETS. EWSR1-FLI1 o EWSR1- ERG sono le traslocazioni più comuni nel ES, osservate rispettivamente nell’85-90% e nel 5-10% di tutti i casi. Altre fusioni geniche sono eccezionalmente rare (meno dell’1% dei casi) e coinvolgono differenti membri della famiglia TET (FUS) ed ETS (ETV1/4, FEV ed E1A-F), come anche riarrangiamenti di EWSR1 con geni della famiglia non ETS (ad es. NFATc2, PATZ1, SMARCA5 e SP3). Le tecniche molecolari, compresa l’analisi FISH e il sequenziamento di nuova generazione, hanno permesso di separare ES con traslocazioni canoniche da un sottoinsieme di lesioni non classificabili, definite nell’ultima classificazione WHO come “sarcomi Ewing-like“ o SBRCT non altrimenti specificati. Anche se un certo numero di SBRCT rimane non classificabile, recenti progressi nella comprensione degli aspetti della biologia molecolare di queste neoplasie hanno reso possibile distinguere entità tumorali in precedenza non riconosciute che ad oggi vengono considerate distinte dall’ES. I sarcomi Ewing-Like con riarrangiamenti di CIC e BCOR sono esempi eclatanti. La diagnosi di queste neoplasie può essere difficile a causa della loro rarità e delle caratteristiche istologiche, ma può essere ottenuta combinando studi morfologici, immunoistochimici e molecolari. L’utilizzo del profilo di metilazione del DNA del tumore è stato suggerito come metodo robusto con un potere straordinario per definire la diagnosi di una coorte di tumori inizialmente identificati come SRBCT non altrimenti specificati.
- Immunoterapia e sarcomi pediatrici
Il primo obiettivo ha permesso di caratterizzare fenotipicamente geneticamente cellule primarie di tumori pediatrici e le linee tumorali immortalizzate in nostro possesso, con il fine di identificare le categorie di pazienti (con espressione elevata della proteina HER3) che potrebbero beneficiare di un innovativo approccio terapeutico.
L’immunoterapia adottiva basata sulle cellule T geneticamente modificate con il CAR-HER3 è un approccio terapeutico promettente in quanto potenzialmente applicabile ad una vasta categorie di pazienti pediatrici con tumori solidi. Inoltre, numerosi autori riportano che l’espressione di questa proteina correla con i tumori ad alto rischio metastatizzati (sarcoma dei tessuti molli) o in fase avanzata (osteosarcoma e NB).
Il recettore tirosin chinasico ERBB3 (HER3) rappresenterebbe, quindi, un target di superficie ideale per un approccio di immunoterapia adottiva per tutti quei pazienti in fase avanzata di malattia, resistenti o refrattari alle terapie convenzionali. Infine, l’introduzione nei nostri CAR di un gene suicida, basato sulla molecola caspasi 9 inducibile, permetterà di ottenere delle cellule T geneticamente modificate clinicamente sicure, in quanto verrebbero velocemente eliminate in caso di eventi avversi (on-target off-tumor) dovuti all’espressione di HER3, pur se a bassi livelli, su alcuni tessuti normali.
* Progetti pubblicati o in corso di revisione grazie al supporto dell’associazione “Il cuore grande di Flavio”
- Circulating Biomarkers for Tumor Angiogenesis: Where Are We? Virginia Di Paolo, Marta Colletti, Valentina Ferruzzi, Ida Russo, Angela Galardi, Iside Alessi, Giuseppe Maria Milano, Angela Di Giannatale. Curr Med Chem. 2020;27(14):2361-2380. doi: 10.2174/0929867325666180821151409.
- Evaluation of Endoglin (CD105) expression in pediatric rhabdomyosarcoma. Di Paolo V, Russo I, Boldrini R, Ravà L, Pezzullo M, Benedetti MC, Galardi A, Colletti M, Rota R, Orlando D, Crocoli A, Peinado H, Milano GM, Di Giannatale A. BMC Cancer. 2018 Jan 5;18(1):31.
- Intraspinal mesenchymal chondrosarcoma: report of a pediatric case and literature review. Di Giannatale A, Colletti M, Russo I, Ferruzzi V, Dell’ Anna VA, Cozza R, Colafati GS, Messina R, Mastronuzzi A, De Vito R, Milano GM. Tumori. 2017 Nov 15;103(Suppl. 1).
- Congenital Rhabdomyosarcoma: a different clinical presentation in two cases. Russo I, Di Paolo V, Gurnari C, Mastronuzzi A, Del Bufalo F, Di Paolo PL, Di Giannatale A, Boldrini R, Milano GM. BMC Pediatr. 2018 May 15;18(1):166.
- Evaluation of Endoglin (CD105) expression in pediatric rhabdomyosarcoma. Di Paolo V, Russo I, Boldrini R, Ravà L, Pezzullo M, Benedetti MC, Galardi A, Colletti M, Rota R, Orlando D, Crocoli A, Peinado H, Milano GM, Di Giannatale A. BMC Cancer. 2018 Jan 5;18(1):31.
- Expression profiles of exosomal miRNAs isolated from plasma of patients with desmoplastic small round cell tumor. Colletti M, Paolini A, Galardi A, Di Paolo V, Pascucci L, Russo I, De Angelis B, Peinado H, De Vito R, Milano GM, Locatelli F, Masotti A, Di Giannatale A. Epigenomics. 2019 Apr;11(5):489-500. doi: 10.2217/epi-2018-0179.Epub2018Dec20.
- A Chart Review on the Feasibility and Safety of the Vincristine Irinotecan Pazopanib (VIPaz) Association in Children and Adolescents With Resistant or Relapsed Sarcomas. Russo I, Di Paolo V, Crocoli A, Mastronuzzi A, Serra A, Di Paolo PL, Di Giannatale A, Miele E, Milano GM. Front. Oncol., 06 August 2020 | https://doi.org/10.3389/fonc.2020.01228
